El hecho de que la demencia se acompañe de alteraciones psicopatológicas y conductuales se conoce desde antiguo. Los gritos, alucinaciones y delirios aparecen ya en la primera descripción de Aloisio Alzheimer de la enfermedad homónima (1) y, con anterioridad, otros autores como Pinel y Esquirol se habían referido a ellos (2).
En 1992, la International Psychogeriatric Association (IPA), en una Conferencia de Consenso (Virginia, EEUU), propuso emplear el término ?Síntomas Psicopatológicos y Conductuales de las Demencias? (SPCD) para referirse a los ?síntomas de alteración de la percepción, del contenido en el pensamiento, el estado de ánimo o la conducta que a menudo se presentan en pacientes con demencia?(3).
Tratamiento farmacológico de los trastornos depresivos en las demencias.
Manuel Martín Carrasco.
Director Médico Clínica Psiquiátrica Padre Menni de Pamplona. Vice-Presidente de la Sociedad Española de Gerontopsiquiatria y Psicogeriatría.
Introducción
El hecho de que la demencia se acompañe de alteraciones psicopatológicas y conductuales se conoce desde antiguo. Los gritos, alucinaciones y delirios aparecen ya en la primera descripción de Aloisio Alzheimer de la enfermedad homónima (1) y, con anterioridad, otros autores como Pinel y Esquirol se habían referido a ellos (2). En 1992, la International Psychogeriatric Association (IPA), en una Conferencia de Consenso (Virginia, EEUU), propuso emplear el término “Síntomas Psicopatológicos y Conductuales de las Demencias” (SPCD) para referirse a los “síntomas de alteración de la percepción, del contenido en el pensamiento, el estado de ánimo o la conducta que a menudo se presentan en pacientes con demencia”(3).
En su concepto actual, entendemos por SPCD una diversa gama de alteraciones psicopatológicas - como ansiedad, depresión, alucinaciones o delirios -, y una inadecuada actividad motora o verbal, no explicables en su totalidad por la satisfacción inmediata de necesidades, o por confusión, que se asocian muy comúnmente al síndrome demencial y que, en muchas ocasiones, son difíciles de tratar.
La detección, diagnóstico y correcto manejo de estos síntomas es sumamente importante, dado que ha quedado claramente establecido en la literatura(4-6) que:
- Contribuyen en gran medida a la sobrecarga de los cuidadores y al ingreso precoz en residencias de los pacientes con demencia.
- Aumentan los costos globales de la demencia. Aunque los costos intangibles del distrés en el paciente y en el cuidador son difíciles de cuantificar, se sabe que el tratamiento de los SPCD es beneficioso tanto en términos económicos como en Años de Vida Ajustados por Calidad.
- Aumentan la incapacidad funcional. Si consideramos que la demencia es una patología altamente productora de discapacidad física, mental y social, es de notable interés eliminar aquellas fuentes adicionales de merma funcional. Los pacientes que presentan SPCD tienen peor rendimiento que los que no los presentan; a su vez, el tratamiento de estos síntomas mejora la capacidad funcional.
- Inducen la utilización de fármacos, a veces de manera inapropiada, que, a su vez pueden contribuir al deterioro funcional, al producir efectos secundarios no deseables.
- Subyacen en algunos casos de abuso y de malos tratos hacia los dementes.
Por todo ello, y a pesar de que tradicionalmente se les ha prestado una atención dentro del estudio de las demencias, en el que se ha primado el deterioro cognitivo, los SPCD constituyen un problema clínico de primera magnitud, probablemente el más importante en la evolución de las demencias.
Los estudios realizados sobre la epidemiología de los SPCD en la enfermedad de Alzheimer (EA) revelan que pueden estar presentes en el 80-90% de los casos, en algún momento de su evolución(7-9). Lo habitual es que se presenten de manera múltiple y diversa; es decir distintos síntomas entremezclados en distintos momentos de la evolución. La recurrencia es la prácticamente la norma, aunque también la recuperación espontánea. Esto equivale a decir que su presentación es oscilante, con apariciones y remisiones, lo que es importante a la hora de valorar la eficacia de los tratamientos y la factibilidad de su retirada.
No se conoce con exactitud la frecuencia relativa de cada uno de los SPCD. Diversos estudios dan cifras muy variables en función de criterios definitorios, población utilizada, tipo y estadio de la demencia, ámbito de realización o método de recogida de datos. En la tabla 1, se puede observar la variabilidad en la frecuencia de algunos síntomas.
Tabla 1. Frecuencia relativa de los SPCD en la enfermedad de Alzheimer en población residente en la comunidad
Como puede apreciarse, las tasas de depresión “per se” en pacientes con enfermedad de Alzheimer que residen en la comunidad son elevadas, pero su prevalencia puede ser aún mayor si tenemos en cuenta que con frecuencia detrás de síntomas como ansiedad o irritabilidad se encuentra un cuadro depresivo. Por otra parte, en trabajos realizados en medio asistencial revelan que la tasa de depresión en la EA puede alcanzar el 20-25% para cuadros de depresión mayor, mientras que hay que considerar otro 20-30% que presentan síntomas depresivos sin entidad suficiente para ser diagnosticados de depresión mayor(12, 13). En el medio residencial(14, 15), la tasa puede alcanzar el 42-50%.
Por lo general, se ha encontrado que la presencia de síntomas depresivos es más frecuente en las fases iniciales o moderadas de la enfermedad, aunque esta observación puede estar influida por la falta de instrumentos para la valoración de estos síntomas en fases avanzadas. No se conoce con exactitud la evolución de los síntomas depresivos en la EA, aunque al menos un trabajo ha encontrado una persistencia del cuadro en el 40% de los casos a los 6 meses(16). Asimismo, se ha descrito que la presencia de antecedentes de trastornos afectivos, tanto personales como familiares, el sexo femenino y el comienzo precoz de la enfermedad son factores de riesgo para la presentación de depresión en la EA(17-20).
En cuanto a la etiología de la depresión en la EA, los conocimientos son escasos, pero la presencia de síntomas depresivos parece correlacionarse más con lesiones específicas de circuitos noradrenérgicos(21) - i. e. locus ceruleus – o serotonérgicos(22) – i. e. núcleos dorsales del rafe – que con la conciencia de enfermedad o el sufrimiento derivado de saber que se la padece(17, 23). Otros hallazgos sugestivos son la correlación entre depresión e hipercortisolemia(24), así como la mayor presencia del alelo ε 4 de la ApoE y depresión en la EA(25), aunque estos datos precisan de una verificación más exacta.
También se ha estudiado la implicación de los lóbulos frontales en la depresión que aparece en la demencia. Por ejemplo, se ha descrito la presencia de lesiones de sustancia blanca en lóbulos frontales de pacientes con demencia – enfermedad de Alzheimer, demencia con cuerpos de lewy, y demencia vascular – y depresión(26), así como de alteraciones del metabolismo de la glucosa en corteza frontal superior bilateral y córtex cingulado anterior izquierdo de pacientes con EA y depresión(27). En cualquier caso, las consecuencias desde el punto de vista clínico de la depresión en la EA son muy importantes, especialmente si tenemos en cuenta que disponemos de tratamientos eficaces. Entre ellas, podemos destacar el empeoramiento de la calidad de vida tanto del paciente como de sus cuidadores, la disminución de la capacidad funcional, el aumento de las conductas agresivas, el aumento del coste de la enfermedad, y un peor pronóstico en cuento a comorbilidad y mortalidad(28-32).
En cuanto a la clínica, los síntomas son similares a los cuadros depresivos habituales en pacientes no demenciados. El problema es que existen síntomas compartidos entre ambas entidades; por ejemplo, la pérdida de apetito y/o de peso, las alteraciones del sueño, los pensamientos reiterativos, o incluso el propio deterioro cognitivo son síntomas típicos de la depresión, pero también de la demencia. Por otra parte, algunos síntomas negativos de la demencia, como la apatía, el embotamiento afectivo o la supresión emocional, pueden dar la falsa apariencia de depresión, aunque su presencia se correlaciona mas con la severidad de la demencia que con la presencia de depresión. Por todo ello, algunos autores recomiendan dar más peso a la hora del diagnóstico de la depresión en la demencia a otras manifestaciones, tales como lloros, tristeza, pensamientos de desesperanza o de inutilidad, así como a la verbalización de ideas de infelicidad o de suicidio(33).
Tratamiento de la depresión en la enfermedad de Alzheimer
Existe una opinión generalizada entre los clínicos que tratan pacientes con demencia que confirma la eficacia de los tratamientos antidepresivos habituales en pacientes con demencia y depresión, si bien dicha opinión no está basada en ensayos clínicos en número y calidad suficientes.
Por otra parte, debemos recordar que los fármacos anticolinesterásicos – sustancias como donepezilo, rivastigmina, y galantamina, indicados en la enfermedad de Alzheimer(34) - reducen de manera significativa la tasa de presentación de estos síntomas(35-37), y especialmente de síntomas como depresión, ansiedad o apatía. Por este motivo, el abordaje correcto de la depresión en la EA consiste en introducir en primer lugar los anticolinesterásicos, y comprobar posteriormente qué síntomas son persistentes y requieren un tratamiento adicional, optando entonces por un tratamiento integral que combine técnicas no farmacológicas con la intervención farmacoterápica, que debe reservarse para un segundo momento, a no ser que la gravedad de la depresión u otros factores, como la presencia de conductas agresivas o de riesgo de suicidio, no hagan aconsejable un abordaje conjunto desde el principio.
En cuanto a las terapias no farmacológicas, es importante incluir en ellas tanto al paciente como a los cuidadores o familiares. Debe comenzarse por establecer un entorno terapéutico adecuado general, abordando temas como la estructuración de horarios, el ejercicio físico, la alimentación, la estimulación cognitiva, y, especialmente la educación del cuidador acerca de los SPCD y la manera de afrontarlos. En cuanto a técnicas específicas, existe sólo información acerca de la terapia cognitiva y conductual, y con un escaso número de trabajos(38-40). En general, se indica que debe emplearse una terapia muy estructurada y dirigida a la resolución de problemas concretos, incluyendo técnicas conductuales dirigidas a incrementar la realización de actividades placenteras y el disfrute obtenido de las mismas. En el único estudio controlado recogido(40), se compararon dos técnicas, una dirigida a los cuidadores y otra hacia los pacientes.
Las dos fueron eficaces a la hora de disminuir los síntomas depresivos de pacientes con EA, comparados con un grupo de pacientes en lista de espera. A pesar de la escasez de trabajos, la falta de riesgos en estas intervenciones y el hecho de que en los ensayos farmacológicos exista una alta tasa de respuesta con placebo, hacen aconsejable que se implementen en primer lugar o de forma conjunta con abordajes farmacológicos, especialmente en los casos más leves.
A la hora de emplear antidepresivos conviene recordar que son especialmente indeseables las sustancias con acción anticolinérgica potente, como la amitriptilina. En general, todos los fármacos antidepresivos tricíclicos – imipramina, clorimipramina, maprotilina – poseen este tipo de acción junto con otras reacciones adversas potencialmente peligrosas (ej. Acción quinidínica, bloqueo alfa-adrenérgico, etc. ), por lo que no deben emplearse en sujetos con demencia. En su lugar conviene emplear fármacos inhibidores de la recaptación de serotonina (ISRS), de los que los más estudiados en demencia, y que cuentan con la ventaja adicional de ser los de primera elección en ancianos dada su tolerabilidad y sus menores interacciones farmacológicas, son la sertralina y el citalopram.
Al margen de sus efectos antidepresivos, parece que son eficaces en el tratamiento de otros SPCD, como la ansiedad, el miedo o la irritabilidad, por lo que están consideradas como fármacos seguros, efectivos y de buena tolerabilidad (6). En estos pacientes, las dosis no se diferencian a las usadas en sujetos deprimidos no demenciados, aunque se recomienda un comienzo a dosis más bajas – por ejemplo, 25 mg/día de sertralina o 10 mg/día de citalopram - e ir aumentando lentamente si es necesario.
Sin embargo, aunque estas recomendaciones son generales y coinciden en ella la mayoría de los autores y recomendaciones de consenso(41-44), están poco apoyadas por estudios rigurosos y comparables(13). Los problemas metodológicos para la comparación de trabajos residen en las diferentes muestras de estudio – por ejemplo, pacientes con deterioro cognitivo, síndrome demencial o EA -, en la heterogeneidad en cuanto a los criterios de diagnóstico, los tamaños de muestra variables, aunque pequeños en general, y la escasa duración de los ensayos.
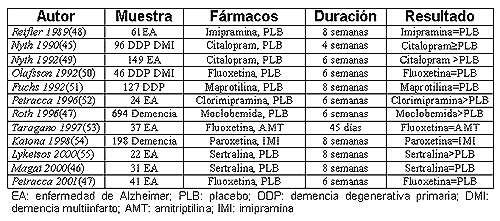
La tabla 2 resume las características fundamentales de los ensayos clínicos realizados hasta ahora en pacientes con demencia o deterioro cognitivo y depresión. Como puede comprobarse, se han realizado 12 estudios controla-dos con antidepresivos en pacientes con demencia y depresión. Los resultados son contradictorios, y no pueden extraerse conclusiones firmes. De los 12 es-tudios, 10 estaban controlados con placebo, y 2 comparaban dos sustancias activas. Dentro de los estudios contra placebo, 5 no encontraban diferencias significativas con placebo, y 5 sí lo hacían, entre ellos el estudio más impor-tante, con 694 pacientes. En términos globales, experimentaron mejoría el 50-75% de los pacientes, con una reducción media del 30-60% en las escalas de evaluación de depresión empleadas. También se apreció por lo general una alta respuesta a placebo, atribuible a la remisión espontánea y al efecto indife-renciado de la atención puesta sobre los síntomas depresivos, tanto en el pa-ciente como en el cuidador.
También hay que destacar que la eficacia de los antidepresivos es mayor conforme aumenta la intensidad de los síntomas de-presivos; ninguno de los tres estudios en los que se incluyeron pacientes con síntomas depresivos leves(45-47) mostraron resultados comparables a place-bo. Dos de los ISRSs probados, sertralina y citalopram, y un inhibidor de la monoaminooxidasa – moclobemida – parecen ser eficaces en el tratamiento de la depresión que aparece en la demencia asociada a la enfermedad de Alzhei-mer. En cuanto a los dos estudios comparativos entre ISRSs y antidepresivos tricíclicos, no se demostraron diferencias en eficacia entre las sustancias com-paradas, aunque los fármacos de segunda generación resultaron mucho mejor tolerados.
Tabla 2. Estudios controlados de depresión en pacientes con demencia
El empleo de otras técnicas, como la terapia electroconvulsiva (TEC), ha sido considerado con mucha cautela en pacientes con demencia, dada la posibilidad de incrementar el déficit de memoria y los posibles efectos deletéreos de la anestesia. En el único estudio que hemos encontrado, una serie retrospectiva de casos, la TEC se mostró como una técnica eficaz y segura, sin originar a medio plazo un aumento del deterioro cognitivo, aunque se producía un aumento de los casos de delirium.
No existen datos publicados acerca del tratamiento a largo plazo de los cuadros depresivos en la EA, por lo que las recomendaciones a seguir suelen ser similares a las seguidas en ancianos no demenciados: mantenimiento del tratamiento al menos durante seis meses posteriormente a la desaparición de los síntomas depresivos, y retirada cautelosa a partir de dicho periodo.
Conclusiones
Los síntomas psicológicos y conductuales de las demencias (SPCD) son muy frecuentes y tienen consecuencias altamente indeseables en términos de coste y de gasto, tanto personales como familiares y sociales. Por lo tanto, su detección y tratamiento es mandatario. Entre estos síntomas destaca la depresión, tanto por su alta prevalencia como por la gravedad de sus consecuencias si no se trata adecuadamente. En este sentido, la literatura no es lo suficientemente contundente en cuanto a pautas de tratamiento, por lo que es necesario profundizar en la investigación en el campo. En el momento actual, la indicación terapéutica consiste en emplear en primer lugar intervenciones no farmacológicas, especialmente en cuadros depresivos leves, para pasar en caso de resistencia o de gravedad al empleo de antidepresivos en primera instancia. Dentro de estos fármacos, los ISRSs son preferibles a los fármacos tricíclicos, aunque la eficacia de ambos tipos de sustancias sea similar, en función de la mejor tolerancia de los primeros.
Bibliografía
1. Alzheimer A. Über eine eigenartige Erkrankunk der Hirnrinde. Allge-meine Zeitschrift für Psychiatrie und Psychisch-Gerichtlich Medizine 1907; 64:146-8.
2. Esquirol JE. Des Maladies Mentales. Paris: Bailière; 1838.
3. Finkel SI CeSJ, Cohen G y cols. Behavioural and psychological signs and symptoms of dementia: a consensus statement on current knowledge and implications for research and treatment. Int Psychogeriatr 1996; 8(Supl 3):497-500.
4. O´Donnell BF DD, Lucas MJ y cols. Incontinence and troublesome behaviors predict Institutionalization in dementia. J Geriatr Psychiatry Neurol 1992; 5:45-52.
5. Ballard CG, O´Brien J, James I, Swam A. Dementia: management of behavioural and psychological symptoms. Oxford: Oxford University Press; 2001.
6. Hemels MEH, Lanctot KL, Iskedjian M, Einarson TR. Clinical and economic factors in the treatment of behavioural and psychological symptoms of dementia. Drugs & Aging 2001; 18:527-50.
7. Mega M, Martin R, Smyth KA, Whitehouse PJ. The spectrum of behavioral changes in Alzheimer's disease. Neurology 1996; 46:130-5.
8. Rao V, Lyketsos CG. Delusions in Alzheimer's disease: a review. J Neuropsychiatry Clin Neurosci 1998; 10(4):373-82.
9. Tariot PN, Erb R, Podgorski CA, Cox C, Patel S, Jakimovich L, , C I. Efficacy and tolerability of carbamazepine for agitation and aggression in dementia. Am J Psychiatry 1998; 155(1):54-61.
10. Burns A, Jacoby R, Levy R. Psychiatric Phenomena in Alzheimer's Disease, IV: Disorders of Behavior. Br J Psychiatry 1990; 157:86-94.
11. Lyketsos CG, Steinberg M, Tschanz JT y cols. Mental and Behavioral Disturbances in Dementia: Findings from the Cache County Study on Memory in Aging. Am J Psychiatry 2000; 157:708-14.
12. Olin JT, Katz IR, Meyers B S, Schneider LS, Lebowitz BD. Provisional diagnostic criteria for depression of Alzheimer disease: rationale and background. Am J Geriatr Psychiatry 2002; 10(2):129-41.
13. Olin JT, Schneider LS, Katz IR, Meyers BS, Alexopoulos GS, , cols BJy. Provisional diagnostic criteria for depression of Alzheimer disease. Am J Geriatr Psychiatry 2002; 10(2):125-8.
14. Brodaty H, Draper B, Saab D, Low LF, Richards V, Paton H, , D L. Psychosis, depression and behavioural disturbances in Sydney nursing home residents: prevalence and predictors. Int J Geriatr Psychiatry 2001; 16(5):504-12.
15. Bell M, Goss AJ. Recognition, assessment and treatment of depression in geriatric nursing home residents. Clin Excell Nurse Pract 2001; 5(1):26-36.
16. Devenand DP, Jacobs DM, Tang M-X y cols. The course of psychopathologic features in mild to moderate Alzheimer's disease. Arch gen Psychiatry 1997; 54:257-63.
17. Migliorelli R, Teson A, Sabe L, Petracchi M, Leiguarda R, , SE S. Prevalence and correlates of dysthymia and major depression among patients with Alzheimer's disease. Am J Psychiatry 1995; 152(1):37-44.
18. Lyketsos CG, Tune LE, Pearlson G, Steele C. Major depression in Alzheimer's disease. An interaction between gender and family history. Psychosomatics 1996; 37(4):380-4.
19. Harwood DG, Barker WW, Ownby RL, Duara R. Association between premorbid history of depression and current depression in Alzheimer's disease. J Geriatr Psychiatry Neurol 1999; 12(2):72-5.
20. Butt ZA, Strauss ME. Relationship of family and personal history to the occurrence of depression in persons with Alzheimer's disease. Am J Geriatr Psychiatry 2001; 9(3):249-54.
21. Zubenko GS. Biological correlates of clinical heterogeneity in primary dementia. neuropsychopharmacology 1992; 6(2):77-93.
22. Forstl H, Burns A, Luthert P, Cairns N, Lantos P, Levy R. Clinical and neuropathological correlates of depression in Alzheimer's disease. Psychol Med 1992; 22(4):877-84.
23. Cummings JL, Ross W, Absher J, Gornbein J, Hadjiaghai L. Depressive symptoms in Alzheimer disease: assessment and determinants. Alzheimer Dis Assoc Disord 1995; 9(2):87-93.
24. O'Brien JT, Ames D, Schweitzer I, Colman P, Desmond P, Tress B. Clinical and magnetic resonance imaging correlates of hypothalamic- pituitary-adrenal axis function in depression and Alzheimer's disease. Br J Psychiatry 1996; 168(6):679-87.
25. Holmes C, Russ C, Kirov G, Aitchison KJ, Powell JF, Collier DA, , S L. Apolipoprotein E: depressive illness, depressive symptoms, and Alzheimer's disease. Biol Psychiatry 1998; 43(3):159-64.
26. Barber R, O'Brien J. Structural and functional magnetic resonance imaging. In: O'Brien J, Ames D, Burns A, editor. Dementia. Londres: Arnold; 2000. p. 115-30.
27. Hirono N, Mori E, Ishii K, Ikejiri Y, Imamura T, Shimomura T, Hashimoto M, Yamashita H, Sasaki M. Frontal lobe hypometabolism and depression in Alzheimer's disease. Neurology 1998; 50(2):380-3.
28. Kales HC, Blow FC, Copeland LA, Bingham RC, Kammerer EE, , AM M. Health care utilization by older patients with coexisting dementia and depression. Am J Psychiatry 1999; 156(4):550-6.
29. Lyketsos CG, Steele C, Galik E, Rosenblatt A, Steinberg M, , Warren A SJ. Physical aggression in dementia patients and its relationship to depression. Am J Psychiatry 1999; 156(1):66-71.
30. McShane R, Keene J, Fairburn C, Jacoby R, Hope T. Psychiatric symptoms in patients with dementia predict the later development of behavioural abnormalities. Psychol Med 1998; 28(5):1119-27.
31. Gonzalez-Salvador MT, Arango C, Lyketsos CG, Barba AC. The stress and psychological morbidity of the Alzheimer patient caregiver. Int J Geriatr Psychiatry 1999; 14(9):701-10.
32. Gonzalez-Salvador T, Lyketsos CG, Baker A, Hovanec L, Roques C, Brandt J, Steele C. Quality of life in dementia patients in long-term care. Int J Geriatr Psychiatry 2000; 15(2):181-9.
33. Martin Carrasco M. Clínica de la enfermedad de Alzheimer. Actas Esp Psychiatr 1999; 27(supl 2):21-33.
34. Cummings JL. Cholinesterase inhibitors: a new class of psychotropic agents. Am J Psychiatry 2000; 157:4-15.
35. Weiner MF, Martin-Cook K, Foster BM, Saine K, Fontaine CS, Svetlik DA. Effects of donepezil on emotional/behavioral symptoms in Alzheimer's disease patients. J Clin Psychiatry 2000; 61(7):487-92.
36. Blesa R. Galantamine: therapeutic effects beyond cognition. Dement Geriatr Cogn Disord 2000; 11 Suppl 1:28-34. EM&action=render&rendertype=fulltext&uid=DEM. dem1a028.
37. Maclean LE, Collins CC, Byrne EJ. Dementia with Lewy bodies treated with rivastigmine: effects on cognition, neuropsychiatric symptoms, and sleep. Int Psychogeriatr 2001; 13(3):277-88.
38. Teri L, Gallagher-Thompson D. Cognitive-behavioral interventions for treatment of depression in Alzheimer's patients. Gerontologist 1991; 31(3):413-6.
39. Teri L. Behavioral treatment of depression in patients with dementia. Alzheimer Dis Assoc Disord 1994; 8(Suppl 3):66-74.
40. Teri L, Logsdon RG, Uomoto J, McCurry SM. Behavioral treatment of depression in dementia patients: a controlled clinical trial. J Gerontol B Psychol Sci Soc Sci 1997; 52(4):159-66.
41. Swartz M, Barak Y, Mirecki I, Naor S, Weizman A. Treating depression in Alzheimer's disease: integration of differing guidelines. Int Psychogeriatr 2000; 12(3):353-8.
42. Boland RJ. Depression in Alzheimer's disease and other dementias. Curr Psychiatry Rep 2000; 2(5):427-33.
43. Gareri P, De Fazio P, De Sarro G. Neuropharmacology of depression in aging and age-related diseases. Ageing Res Rev 2002; 1(1):113-34.
44. Lyketsos CG, Olin J. Depression in Alzheimer's disease: overview and treatment. Biol Psychiatry 2002; 52(3):243-52.
45. Nyth AL, Gottfries CG. The clinical efficacy of citalopram in the treatment of emotional disturbances in dementia disorders: A Nordic multicentre study. Br J Psychiatry 1990; 157:894-901.
46. Magai C, Kennedy G, Cohen CI, Gomberg D. A controlled clinical trial of sertraline in the treatment of depression in nursing home patients with late-stage Alzheimer's disease. Am J Geriatr Psychiatry 2000; 8(1):66-74.
47. Petracca GM, Chemerinski E, Starkstein SE. A double-blind, placebo-controlled study of fluoxetine in depressed patients with Alzheimer's disease. Int Psychogeriatr 2001; 13(2):233-40.
48. Reifler BV, Teri L, Raskind M, Veith R, Barnes R, White E, McLean P. Double-blind trial of imipramine in Alzheimer's disease patients with and without depression. Am J Psychiatry 1989; 146(1):45-9.
49. Nyth AL, Gottfries CG, Lyby K, Smedegaard-Andersen L, Gylding-Sabroe J, Kristensen M, Refsum HE, Ofsti E, Eriksson S, , S S. A controlled multicenter clinical study of citalopram and placebo in elderly depressed patients with and without concomitant dementia. Acta Psychiatr Scand 1992; 86(2):138-45.
50. Olafsson K, Jorgensen S, Jensen HV, Bille A, Arup P, Andersen J. Fluvoxamine in the treatment of demented elderly patients: a double- blind, placebo-controlled study. Acta Psychiatr Scand 1992; 85(6):453-6.
51. Fuchs A, Hehnke U, Erhart C, Schell C, Pramshohler B, Danninger B, Schautzer F. Video rating analysis of effect of maprotiline in patients with dementia and depression. Pharmacopsychiatry 1993; 26(2):37-41.
52. Petracca G, Teson A, Chemerinski E, Leiguarda R, Starkstein SE. A double-blind placebo-controlled study of clomipramine in depressed patients with Alzheimer's disease. J Neuropsychiatry Clin Neurosci 1996; 8(3):270-5.
53. Taragano FE LC, Mangone CA, Allegri RF, Comesana-Diaz E. A double-blind, randomized, fixed-dose trial of fluoxetine vs. amitriptyline in the treatment of major depression complicating Alzheimer's disease. Psychosomatics 1997; 38(3):246-52.
54. Katona CL, Hunter BN, Bray J. A double-blind comparison of the efficacy and safely of paroxetine and imipramine in the treatment of depression with dementia. Int J Geriatr Psychiatry 1998; 13(2):100-8.
55. Lyketsos CG, Sheppard JM, Steele CD, Kopunek S, Steinberg M, Baker AS, Brandt J, Rabins PV. Randomized, placebo-controlled, double-blind clinical trial of sertraline in the treatment of depression complicating Alzheimer's disease: initial results from the Depression in Alzheimer's Disease study. Am J Psychiatry 2000; 157(10):1686-9
IMPORTANTE: Algunos textos de esta ficha pueden haber sido generados partir de PDf original, puede sufrir variaciones de maquetación/interlineado, y omitir imágenes/tablas.

Antidepresivos glutamatérgicos: nueva perspectiva de tratamiento rápido de los trastornos depresivos con esketamina
Samuel Pombo Chorto
Fecha Publicación: 21/05/2021
Utilización de antipsicóticos y antidepresivos en asociación: revisión bibliográfica.
Ignacio Muñoz Siscart
Fecha Publicación: 24/12/2012
Adicción sexual y trastornos depresivos.
Maria Bernarda Romero
Fecha Publicación: 01/03/2007