Bases neurobiológicas de las asociaciones de antidepresivos.
Francisco Ferre.
Departamento Asistencia Psiquiátrica y Salud Mental.
Comunidad de Madrid.
Introducción
Seguramente los psiquiatras cuando hacemos psicofarmacología empírica o “creativa” y ajustamos dosis, combinamos psicofármacos o añadimos un nuevo agente a una pauta establecida, estamos inspirados en nuestra intuición, nuestra experiencia previa y nuestros conocimientos. Esta forma de abordar el tratamiento farmacológico de los enfermos mentales seguirá existiendo durante mucho tiempo. Sin embargo parece conveniente y útil que tengamos un sustrato teórico sobre el que plantearse nuevos modos de usar los psicofármacos. Ese sustrato crece día a día conforme la psicofarmacología experimental ayudada de las nuevas técnicas de neuroimagen, nos ofrece más evidencias sobre el funcionamiento del cerebro en los trastornos mentales y su tratamiento. Por todo ello es imprescindible que el psiquiatra tenga nociones claras sobre lo que se conoce acerca de la Neurobiología de la enfermedad mental y su tratamiento farmacológico.
En la depresión y todo su espectro se dan varias circunstancias que hacen especialmente trascendente tener esos conocimientos. Se trata de una enfermedad de larga evolución y por lo tanto los fármacos se utilizan durante mucho tiempo. Existe una amplísima gama de antidepresivos y pautas de administración. Los casos refractarios al tratamiento exigen un esfuerzo diagnóstico y psicofarmacológico importante.
En efecto, los psiquiatras recurrimos a las asociaciones de antidepresivos buscando alcanzar efectos neuroquímicos diversos, sobre el denominador común de que “dos mecanismos son más potentes que uno sólo”, lo cual, por el hecho de que a menudo resulte clínicamente eficaz, no quiere decir que sea neurobiológicamente cierto .
El uso de la combinación de antidepresivos tiene su razón de ser en tres motivos:
- algunas combinaciones de antidepresivos pueden fomentar sinergias moleculares que potencien la neurotransmisión monoaminérgica
- algunas combinaciones se han hecho populares en cuanto a su seguridad y eficacia a raíz de casuística no controlada en la práctica clínica
- la utilización de terapia combinada de fármacos como abordaje de problemas médicos de difícil solución (por ejemplo el SIDA, cáncer o hipertensión resistente) , incluye a problemas psiquiátricos
Diferentes observaciones han asociado la administración conjunta de dos antidepresivos a cambios neuroquímicos potentes que podrían justificar una mayor respuesta clínica. Por ejemplo, la administración conjunta de fluoxetina y desipramina se asocia a una rápida “down-regulation” de los adrenoreceptores beta, que justificaría un alivio mayor y más rápido en determinados casos .
La asociación de paroxetina y mirtazapina da lugar a una activación serotoninérgica mayor y más rápida, lo cual se pone de manifiesto en la mayor activación mayor y más rápida de los receptores 5. HT1a postsinápticos en el cerebro de rata. Este mecanismo se podría relacionar con la potenciación y aceleración de la respuesta antidepresiva .
El problema de nuevo es que a menudo no es posible comprobar si tales efectos se producen realmente, y si son los responsables de la “potenciación” de la respuesta antidepresiva. Esto último es especialmente difícil de justificar, sobre todo si tenemos en cuenta que hoy día sabemos lo suficiente como para separar el efecto de un antidepresivo sobre un determinado sistema de neurotransmisión, o sobre ciertos receptores, y el mecanismo por el que se produce el efecto clínico, el cual dependería en último extremo de una vía final común relacionada con segundos y terceros mensajeros, que dan lugar a modificaciones de las actividades genómicas y de la síntesis proteica intracelular.
En definitiva resulta difícil justificar la utilidad de una u otra combinación sobre la base de fundamentos neuroquímicos sólidos. Por lo tanto, la mayor parte de las veces tenemos que contentarnos con justificaciones clínicas y guiarnos por observaciones empíricas.
Bases neurobiológicas de la acción antidepresiva
Desde un punto de vista neurobiológico un fármaco para producir un efecto clínico específico debe:
- Actuar sobre un lugar de acción fisiológicamente relevante para el efecto. Este lugar puede ser una bomba de recaptación, un receptor o una enzima.
- Reconocer dicho lugar de acción, activar(agonista) o inhibir(antagonista) y producir un cambio en la actividad celular
NEUROBIOLOGÍA DE LA DEPRESIÓN
Aunque se han postulado teorías que encontraban en un solo neurotransmisor la explicación del funcionamiento cerebral en la depresión, hoy han quedado desechadas por simplistas y existe cierto acuerdo en admitir que la depresión desde el punto de vista neurobiológico sería consecuencia del anormal funcionamiento de varios neurotransmisores.
Sin embargo, para conseguir los objetivos didácticos de esta monografía, recordaremos lo esencial de la hipótesis monoaminérgica de la depresión y el modo de funcionamiento de los neurotransmisores más importantes en esta enfermedad.
Siendo cada día más evidenciable que la depresión se produce por una disfunción de la neurotransmisión cerebral podemos admitir que:
-. Aunque los neurotransmisores funcionen fisiológicamente los receptores pueden tener una respuesta inadecuada
-. Funcionando correctamente neurotransmisor, receptor y respuesta de éste, el problema se podría localizar a nivel del segundo mensajero que intracelularmente traduce el “mensaje” neuroquímico.
-. El segundo mensajero altere la formación de factores de transcripción intracelular que a su vez controlan la regulación génica de las neuronas, en concreto del hipocampo.
HIPÓTESIS MONOAMINÉRGICA
Según esta hipótesis con la que hemos trabajado durante tres décadas, la depresión se produciría por déficit de la noradrenalina, la serotonina y /o la dopamina:
- Estado normal: se libera a velocidad normal al monoamina, se metaboliza por la MAO , es retirada de la sinapsis por la bomba de recaptación y finalmente los receptores postsinápticos responden.
- Estado depresivo: hay una anomalía en los receptores de los neurotransmisores monoamínicos que puede ser causado a su vez por la disminución de neurotransmisores
- proceso neurobiológico: la falta de neurotransmisores hace que los receptores aumenten en número (regulación al alza) y esto significaría depresión.
- Cuando se administra un fármaco que detiene la degradación de la monoamina (IMAO) o la bomba de recaptación , aumentará la disponibilidad de neurotransmisor y esto coincide con la acción antidepresiva.
SISTEMAS NEUROTRANSMISORES IMPLICADOS EN LA DEPRESIÓN
. NORADRENALINA
Los reguladores de la noradrenalina son: las enzimas metabolizadoras mono amino oxidasa(MAO )y la catecol- orto-metil transferfasa( COMT); y la bomba de recaptación que es una bomba de transporte selectiva para la noradrenalina que barre este neurotransmisor del espacio intersináptico.
Los receptores se sitúan a nivel postsináptico (el beta 1 y los adrenérgicos alfa 1 y alfa 2) que son los que operativizan la neurotransmisión y a nivel presináptico (alfa 2) que impide la liberación de noradrenalina y por lo tanto frena la neurona noradrenérgica.
. DOPAMINA
La dopamina es degradada por las mismas enzimas que la noradrenalina y la neurona dopaminérgica tiene un transportador presináptico (bomba de recaptación) que es selectivo para la dopamina.
Los receptores son al menos 5 subtipos farmacológicos siendo el más investigado y conocido el D2 que es el que se estimula con agonistas en el tratamiento de la enfermedad de Parkinson y es el bloqueado por los neurolépticos antagonistas de la la dopamina en el tratamiento de la esquizofrenia.
. SEROTONINA
La serotonina es metabolizada por la enzima MAO y la neurona serotoninérgica tiene una bomba de recaptación presináptica. Se han caracterizado un buen número de receptores serotoninérgicos:
- Presinápticos : 5HT1A y 5HT1D
- Postsinápticos: 5HT1A , 5HT1D, 5HT2A 5HT2C, 5HT3, 5HT4 y otros
Los 5HT1A son autorreceptores (sólo aceptan el neurotransmisor de su neurona, en este caso serotonina) y por su localización se llaman somatodendríticos. Puede ser presináptico y controla la liberación de serotonina cuando experimenta regulación a la baja produce mayor liberación de serotonina. Y puede ser postsináptico donde se genera parte de la neurotransmisión serotoninérgica y además desempeña un importante papel en la termorregulación. Es este un receptor que contribuye en gran medida al perfil terapéutico de los ISRS.
Los 5HT1D de la terminación axonal presináptica cuando son estimulados bloquean la liberación de serotonina.
Un tercer receptor inhibidor de la neurona serotoninérgica es el alfa 2 presináptico localizado en la terminación axónica. Puede inhibir la liberación de serotonina cuando es ocupado por la noradrenalina, por eso es denominado heterorreceptor.
Si los tres receptores se ocupan simultáneamente la serotonina puede ser liberada.
El receptor postsináptico 5HT2A cuando es estimulado causa agitación, acatisia, ansiedad, insomnio y disfunción sexual, si bien este receptor se cree es fundamental en la actividad terapéutica de los ISRS. El receptor 5HT3 cuando se estimula causa los efectos secundarios gastrointestinales de los ISRS.
. INTERACCIÓN SEROTONINA- NORADRENALINA
Hay dos tipos de interacciones:
- Presináptica: la noradrenalina actúa como freno de la liberación de serotonina
o Axo-axónica
o Autorreceptor alfa2 terminal
- Postsináptica : la noradrenalina acelera la liberación de serotonina
o Axo-dendrítica
o 5-somatodendrítica
o receptores alfa 1 excitadores
Farmacodinamia de los antidepresivos
Los antidepresivos producen primero cambios en los neurotransmisores, luego cambios en el estado de ánimo y finalmente cambios en la sensibilidad del receptor. La cantidad de neurotransmisor cambia pronto tras la toma del antidepresivo, pero el efecto clínico de mejoría se retrasa hasta que se produce la regulación a la baja del receptor del neurotransmisor.
ANTIDEPRESIVOS HETEROCÍCLICOS (conocidos como tricíclicos)
El uso de estos fármacos suponen cinco mecanismos de acción:
- inhibición de la recaptación de serotonina: bloqueando la bomba de recaptación de serotonina, consigue acción antidepresiva
- inhibición de la recaptación de noradrenalina: bloqueando la bomba de recaptación de noradrenalina, obtiene acción antidepresiva
- Fármaco anticolinérgico-antimuscarínico que produce aumento de peso, somnolencia, estreñimiento y visión borrosa
- antagonista alfa 1 adrenérgico: produciendo hipotensión, mareo y somnolencia
- Antihistamínico
INHIBIDORES SELECTIVOS DE LA RECAPTACIÓN DE SEROTONINA (ISRS)
El proceso farmacodinámico es el siguiente:
1º En el paciente depresivo hay un déficit del neurotransmisor serotonina y el número de receptores serotoninérgicos se regulan al alza aumentando tanto los autorreceptores presinápticos como los postsinápticos.
2º El ISRS bloquea de inmediato la bomba de recaptación de serotonina y se genera un incremento de la serotonina en la zona somatodendrítica pero no en las terminaciones axónicas.
3º La elevación de la serotonina en la zona somatodendrítica regula a la baja el número de autorreceptores 5HT1A .
4º Al disminuir los 5HT1A , éstos dejan de inhibir los impulsos de la neurona serotoninérgica y comienza a liberarse más serotonina en la terminación axónica.
5ºFinalmente como consecuencia de la liberación de serotonina se acaba produciendo una regulación a la baja de los receptores serotoninérgicos postsinápticos.
Todo este proceso es lento y probablemente es lo que explique el período de latencia de respuesta a la depresión de estos fármacos.
INHIBIDOR DE LA RECAPTACIÓN DUAL (Venlafaxina)
Combina las acciones de inhibidor de la recaptación de serotonina con la de inhibición de la recaptación de noradrenalina y con cierto bloqueo de la recaptación de dopamina.
Carece de 3 de los 5 mecanismos de acción que tenían los antidepresivos tricíclicos y no tienen acción alfa adrenérgico, acción antihistamínica ni acción anticolinérgica.
Parece ser que a dosis bajas de antidepresivo se produce exclusivamente la inhibición de la serotonina; que a dosis intermedias se consigue la inhibición de noradrenalina y serotonina y finalmente a dosis muy elevadas , se obtiene la inhibición de la recaptación de noradrenalina, de serotonina y de dopamina también.
ANTAGONISTA DE receptores ALFA 2 ADRENÉRGICOS (Mirtazapina)
Este fármaco actúa con cuatro acciones:
1º Antagoniza el receptor alfa 2 presináptico que inhibe la liberación de noradrenalina y de serotonina. De tal forma que al ser antagonizado se produce un incremento de la neurotransmisión de noradrenalina y serotonina.
2º Antagonismo de los receptores 5HT2. Como estos receptores serotoninérgicos son los que median efectos secundarios de los ISRS como ansiedad e insomnio, resulta una optimización de su tolerabilidad
3º Antagonismo de los receptores 5HT3 . Estos receptores son los implicados en los efectos adversos gastrointestinales de los ISRS por lo tanto con esta acción desaparecen dichos efectos.
4º Antihistaminérgico, lo cual disminuye la ansiedad por un lado pero puede aumentar la probabilidad de incremento de peso y algo de sedación.
En definitiva tiene acción dual noradrenalina / serotonina sin tener que bloquear las bombas de recaptación.
INHIBIDOR SELECTIVO DE LA RECAPTACIÓN DE noradrenalina (Reboxetina)
Tiene una acción selectiva inhibiendo la bomba de recptación noradrenérgica de las neuronas adrenérgicas.
INHIBIDOR DE LA RECAPTACIÓN DE noradrenalina Y DOPAMINA (Bupropion)
Este fármaco inhibe las bombas de recaptación tanto de noradrenalina como de dopamina.
RESUMEN DE CORRESPONDENCIA CLÍNICA CON LOS PRINCIPALES MECANISMOS DE ACCIÓN ANTIDEPRESIVA:
Implicaciones de la farmacocinética en el uso de antidepresivos
A) FARMACOCINÉTICA GENERAL
Si la farmacodinamia es la manera en que los fármacos actúan sobre el organismo, la farmacocinética sería la forma en que el organismo actúa sobre el fármaco.
Los aspectos de la farmacocinética de los antidepresivos que debemos conocer son:
1º Absorción:
- vía de absorción
- factores que alteran : motilidad gástrica e intestinal
- alimentos que favorecen o impiden la absorción
- velocidad de absorción
- biodisponibilidad: el porcentaje de antidepresivo administrado que alcanza el territorio venoso más allá del hígado y por ello el porcentaje de fármaco disponible para actuar en su lugar de acción. Este concepto no tiene utilidad práctica
2º Distribución:
- fijación a proteínas: el antidepresivo en sangre quedará parte unido a proteínas y parte en fracción libre que es la que puede variar la respuesta farmacológica.
- Volumen de distribución: el volumen total de agua corporal por el que se distribuye un fármaco y este valor es propio de cada sustancia. El antidepresivo cuando llega al cerebro, se redistribuye por el resto del organismo. Si el volumen de distribución es bajo, las concentraciones cerebrales y el tiempo que se mantendrán serán mayores que en otro fármaco que tenga un volumen de distribución elevado.
3º Eliminación:
-los fármacos hidrosolubles son excretados por filtración glomerular o secreción tubular activa a través del riñón. Los fármacos no hidrosolubles deben ser metabolizados con sistemas enzimáticos localizados en el hígado
- Vida Media: es el tiempo que la concentración máxima alcanzada por un fármaco tras una administración única tarda en disminuir a la mitad. Los antidepresivos de vida media larga presentarán mayor duración de los efectos incluidos los adversos
4º Metabolización hepática:
- El antidepresivo ingerido accede al intestino y actuará como sustrato para las isoenzimas hepáticas del citocromo P450 produciéndose una biotransformación, de tal manera que el antidepresivo pueda ser excretado y eliminado.
- Se conocen varias isoenzimas del citocromo P450 : IA2; IID6; IIIA3/4; y IIC19. Pero no todos los individuos tienen las mismas isoenzimas del citocromo P 450. De hecho 2 de cada 20 personas de raza blanca carecen de la isoenzima IID6 y metabolizan los fármacos por otras vías no tan eficientes.
- CYPIID6: ha sido la más estudiada, hay un grupo de metabolizadores lentos en relación al déficit congénito ya referido en 10% de la población. Los metabolizadores lentos mostrarán con algunos fármacos vidas medias muy alargadas, grandes concentraciones plasmáticas y exageradas respuestas farmacológicas. Metaboliza antidepresivos, antipsicóticos, bloqueantes beta adrenérgicos, antiarrítmicos tipo IC, dextrometorfano, codeína y algunos agentes quimioterápicos. En relación a los antidepresivos la inhibición que producen de más a menos es: paroxetina> norfluoxetina>fluoxetina>sertralina> fluvoxamina> venlafaxina > mirtazapina (Richelson 1997)
- CYP3A4: es considerada la más importante clínicamente. No tiene polimorfismo genético. Metaboliza alprazolam, terfenadina, astemizol, cisapride, carbamazepina, sertralina, antidepresivos tricíclicos, bloqueadores de canales del calcio, ciclosporina, eritromicina, esteroides, codeína , quinidina , lidocaína , zumo de pomelo , ketoconazol y verapamilo entre otros. El gradiente de potencia inhibitoria de los antidepresivos es : fluvoxamina>norfluoxetina> paroxetina>desmetilsertralina>fluoxetina>sertralina>mirtazapina>>>>venlafaxina
- CYP I A2: el 12% de la población son metabolizadores lentos. Su actividad aumenta con el humo de los cigarrillos, las comidas a la brasa, y la coliflor. Metaboliza acetominofeno, cafeína, clozapina, haloperidol, propranolol, fenotiazinas, fenacetina, tríciclicos, teofilina y warfarina. La inhibición que producen los antidepresivos es así: fluovoxamina>>paroxetina=sertralina>fluoxetina=norfluoxetina>mirtazapina>>>venlafaxina.
- CYP IIC: tiene las subfamilias 2C9, 2C10 y 2C19. Esta última es la que exhibe polimorfismo genético y 18% de japoneses, 19% de afroamericanos , 8% de africanos y 3-5% de caucasianos son metabolizadores lentos. Metaboliza diacepam, citalopram, tricíclicos, warfarina, fenitoína, omeprazol, tolbutamida y algunos AINES. No existe precisa información sobre el poder inhibitorio de los antidepresivos aunque se sabe que tanto fluvoxamina como fluoxetina son inhibidores .
B) INTERACCIONES FARMACOCINÉTICAS
B. 1 A NIVEL DE LA ABSORCIÓN
Son poco frecuentes, pero interesa saber que los fármacos con acción anticolinérgica disminuyen la biodisponibilidad de antidepresivos como los tricíclicos cuya absorción depende de la motilidad intestinal.
B. 2 A NIVEL DE LA DISTRIBUCIÓN
Es raro que ocurra y debe ser con dosis muy elevadas del antidepresivo por ejemplo los ISRS que se fijan intensamente a proteínas y pueden desplazar a anticoagulantes como la warfarina
B. 3 A NIVEL DE LA METABOLIZACIÓN HEPÁTICA
Si un fármaco inhibe las isoenzimas del citocromo P450 que metabolizan a un antidepresivo , aumentarán las concentraciones del fármaco activo y potenciará su actividad antidepresiva pero también incrementará los efectos adversos. Por eso a efectos de prevención farmacocinética conviene recordar que:
- A nivel del CYPIA2:
o La fluvoxamina puede incrementar los niveles de teofilina y clozapina
o La combinación de grandes cantidades de zumo de pomelo y antibióticos como la ciprofloxacina y norfloxacina pueden incrementar los niveles de éstos últimos
- A nivel CYP IID6:
o Los ISRS pueden aumentar los niveles de antidepresivos heterocíclicos, lo cual puede ser interesante para la asociación y potenciación de la acción antidepresiva, pero también puede tener consecuencias en lo referente a los efectos adversos de los tricíclicos.
o Los ISRS pueden bloquear el efecto analgésico de la codeína e incrementar sus niveles
o Los ISRS pueden aumentar los niveles de los beta bloqueantes
- A nivel CYP3A4:
o La combinación ketoconazol o eritromicina con terfenadina , astemizol o cisaprida podría ser letal
o Hay que evitar la combinación de los fármacos referidos con fluvoxamina y posiblemente fluoxetina y otros ISRS
o La carbamazepina es sustrato e inductor a la vez de este citocromo. Cuando se inicia el tratamiento los niveles plasmáticos de la carbamazepina reflejan la actividad basal CYP3 A 4 pero pasado el tiempo el incremento de la actividad enzimática aumenta el metabolismo del fármaco y debe vigilarse.
B-4 INTERACCIONES A NIVEL DE citocromo P450 DE LOS NUEVOS ANTIDEPRESIVOS
- VENLAFAXINA
o Se ha comparado con fluoxetina y paroxetina la inhibición que producen al CYPIID6 con dextrometrofano y venlafaxina no aumenta los niveles de este sustrato
o Aunque venlafaxina no afecta la farmacocinética de la imipramina, sin embargo el metabolito activo de la imipramina si se vió alterado y la desipramina aumentó el 35% de su nivel plasmático en presencia de venlafaxina. Por lo tanto hay que tener precaución en esta combinación.
o Asociado con la terfenadina, no existe ninguna alteración farmacocinética
- MIRTAZAPINA
o Aunque es un débil inhibidor de las isoenzimas IA2; IID6; y IIIA4, tiene un muy bajo potencial de producir interacciones clínicamente significativas
Posibles fundamentos de la asociación de antidepresivos
PRINCIPIOS DE LA COMBINACIÓN DE ANTIDEPRESIVOS
1º Se deben combinar mecanismos de acción no simplemente fármacos. Los psicofármacos son simplemente portadores de mecanismos de acción farmacodinámicos. Por eso cuando combinamos dos antidepresivos , a veces estamos combinando tres o más mecanismos de acción. Por otro lado disponemos de psicofármacos distintos que ofrecen los mismos mecanismos de acción (por ejemplo los ISRS)
2º Se deben perseguir combinaciones sinérgicas y no exactas matemáticamente. Es decir una combinación exitosa es la que en términos de eficacia multiplica la acción antidepresiva no la que simplemente añade (interesa 1+1=10 y no el 1+1=2); y en términos de tolerabilidad de los efectos adversos minimiza los mecanismos de acción (1+1=0). Lógicamente lo ideal sería multiplicar eficacia y neutralizar secundarismos.
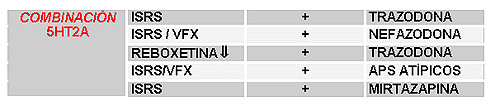
3º Se deben explotar al máximo las posibilidades de combinación de mecanismos de acción, incluso asociando dos acciones farmacológicamente independientes pero que cada una de ellas sean a su vez sinérgicas con los sistemas noradrenérgicos, serotoninérgicos e incluso dopaminérgicos. Un ejemplo de ello es la combinación del bloqueo de la recaptación de serotonina (ISRS) con el antagonismo de los receptores serotoninérgicos 2 A (trazodona o nefazodona)
SINERGIAS CON EL SISTEMA SEROTONINÉRGICO
La potenciación de la neurotransmisión serotoninérgica ha resultado ser útil no sólo en la depresión resistente sino que también en la resistencia al tratamiento de los trastornos del espectro serotoninérgico: trastorno obsesivo compulsivo, crisis de ansiedad, fobia social, trastorno por estrés postraumático y bulimia.
Un ejemplo característico es la estrategia de antagonismo del receptor serotoninérgico 2 A (5HT2A). Para esta estrategia se combinaría una intensa inhibición de la recaptación de la serotonina y una intensa inhibición de los receptores 5HT2A.
Quizás el ejemplo de esta estrategia más frecuente es el resultante de la asociación de trazodona y un ISRS. Los clínicos asumen que la trazodona corrige el insomnio y la agitación que pudieran producir los ISRS y eso les permitiría utilizar dosis muy altas de ISRS no sólo en depresión sino en trastorno obsesivo compulsivo y otros trastornos de ansiedad.
Respecto a la combinación mirtazapina y paroxetina Montigny (1998) informa que el tratamiento a largo plazo con mirtazapina aumenta la actividad del las neuronas serotoninérgicas del rafe dorsal y la neuronas noradrenérgicas del locus coeruleus y además desensibiliza los adrenoreceptores alfa 2 localizados en las terminales serotoninérgicas. El tratamiento a largo plazo con paroxetina desensibiliza los receptores somatodendríticos 5HT1A y los atutoreceptores terminales 5HT1B, y además regula a la baja los transportadores de serotonina. Todo ello según este autor que lo analizó en el cerebro de rata, podría dar lugar no sólo a una respuesta antidepresiva más eficaz, sino sobre todo a una aceleración de la respuesta.
SINERGIAS CON LA NORADRENALINA
La potenciación de la neurotransmisión noradrenérgica puede ser útil no sólo en la depresión en general sino en los respondedores parciales con síntomas persistentes de apatía, fatiga y elentecimiento cognitivo.
Los inhibidores selectivos de la recaptación de la noradrenalina como la reboxetina pueden combinarse con un dopaminérgico-noradrenérgico como el bupropion. Así mismo el bupropion o la reboxetina podrían combinarse con un liberador de dopamina como el metilfedinato o con el agonista dopaminérgico llamado pramipexol. Esta estrategia es especialmente útil en pacientes con depresión melancólica o inhibida y en aquellos trastornos bipolares que precisan un antidepresivo concomitante con el estabilizador del ánimo.
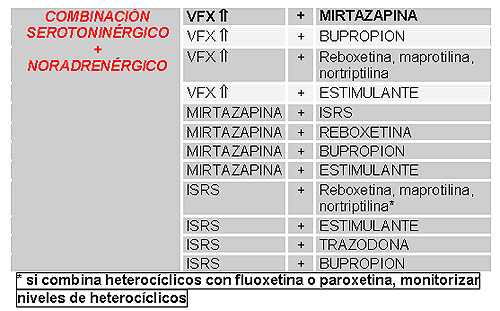
POTENCIACIÓN SEROTONINA Y NORADRENALINA
En los pacientes más refractarios resulta necesaria la combinación serotoninérgica y noradrenérgica. :
Bibliografía
-Fava M. New approaches to the treatment of refractory depression. J Clin Psychiatry. 2000; 61 (suppl1) ; 26-32
-Fischer P, Tauscher J, Kuefferle B, Kasper S. Weak antidepressant response after buspirone augmentation of serotonin reuptake inhibitors in refractory severe depression. Int Clin Psychopharmacol. 1998; 13: 83-86
-Gibert Rahola J. Lo que siempre quiso saber de los psicofármacos… y nunca se atrevió a preguntar. Gibert J Eds. Aula Medica Madrid 2000
-Greenblatt DJ, von Moltke LL; Harmatz JS; Shader RI. Drug interactions with newer antidepressants: role of human cytochromes P450. J Clin Psychiatry. 1998; 59(suppl15) 19-27
-Owen JR, Nemeroff CB. New antidepressants and the cytochrome P450 system: focus on venlafaxine, nefazodone and mirtazapine. Depression and Anxiety. 1998, 7suppl 1: 24-32
- Preskorn SH. Targeted pharmacoterapy in depresión management:pharmacokinetics of fluoxetine, paroxetine and sertraline. Int Clin Psychopharmacol 1994 ; 9(suppl 3): 13-19
-Richelson E. Pharmacokinetic drug interactions of new antidepressants: A review of the effects on the metabolism of other drugs. Mayo Clin Proc ; 1997; 72: 835-847
-Stahl SM. Psicofarmacología de los antidepresivos. Martín Dunitz Eds. Londres 1997
IMPORTANTE: Algunos textos de esta ficha pueden haber sido generados partir de PDf original, puede sufrir variaciones de maquetación/interlineado, y omitir imágenes/tablas.





Asociaciones de antidepresivos: resultados de una encuesta de opinión de psiquiatras españoles.
J. Vicente García
Fecha Publicación: 01/01/2003